原题:
27(10分)A、B、C、D、E均为中学中学化学中的常见物质,它们之间的反应关系如下图所示:
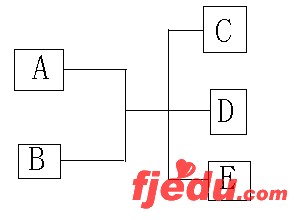
(1)(2)(3)略
(4)若C为氧气,D、E的焰色反应均呈黄色,E与盐酸反应生成的气体能使澄清石灰水变浑浊,则n(A)与n(B)的关系为 。
答案与讨论:
本题的答案为n(A):n(B)≥1,得出此答案的前提是推出A为Na2O2,B为NaHCO3,C为O2,D为NaOH,E为Na2CO3,解答本题的思路有以下两种:
(1)Na2O2先与H2O反应,化学方程式为:2Na2O2+2H2O=4NaOH+O2 ,生成的NaOH再与NaHCO3反应,化学方程式为:NaOH+ NaHCO3== Na2CO3 +H2O,这样只要Na2O2的量为NaHCO3的量的一半以上,产物中就有O2、、NaOH和Na2CO3,同时有水,那此时的答案就应该是n(A):n(B)>1/2。
(2)2Na2O2+ 2NaHCO3====2Na2CO3+ O2+2NaOH,只有n(A):n(B)≥1,产物中才会只产生三种物质O2、、NaOH和Na2CO3(此时只有三种物质生成,没有水生成)。
综上所述,可以得出以下结论:
n(A):n(B)≤1/2,则产物只有三种:O2、Na2CO3和H2O,没有NaOH,不合题意;
1/2<n(A):n(B)<1,则产物有四种:O2、、NaOH、Na2CO3及H2O,是不是符合题意值得讨论;
n(A):n(B)≥1,则产物中有三种:O2、、NaOH、Na2CO3,一定符合题意。
笔者认为此题是好题,但有一定难度。我认为以下问题值得讨论:
(1)反应中生成的水一定要当作第四种产物吗?本题的已知条件中B是溶液,可能学生在解题时会认为水的生成可以不考虑。这样造成解答时出现错误。
(2)Na2O2与NaHCO3的反应是直接反应还是Na2O2先与水反应,生成的NaOH再与NaHCO3反应,学生在解答这样的问题时可能不能完全按照出题者的意思解答。在溶液中Na2O2与NaHCO3的反应,一定要按照以上解法(2)所示的化学方程式进行,而不能按解法(1)所示的化学方程式进行,笔者认为有点强加于学生,不够妥当。